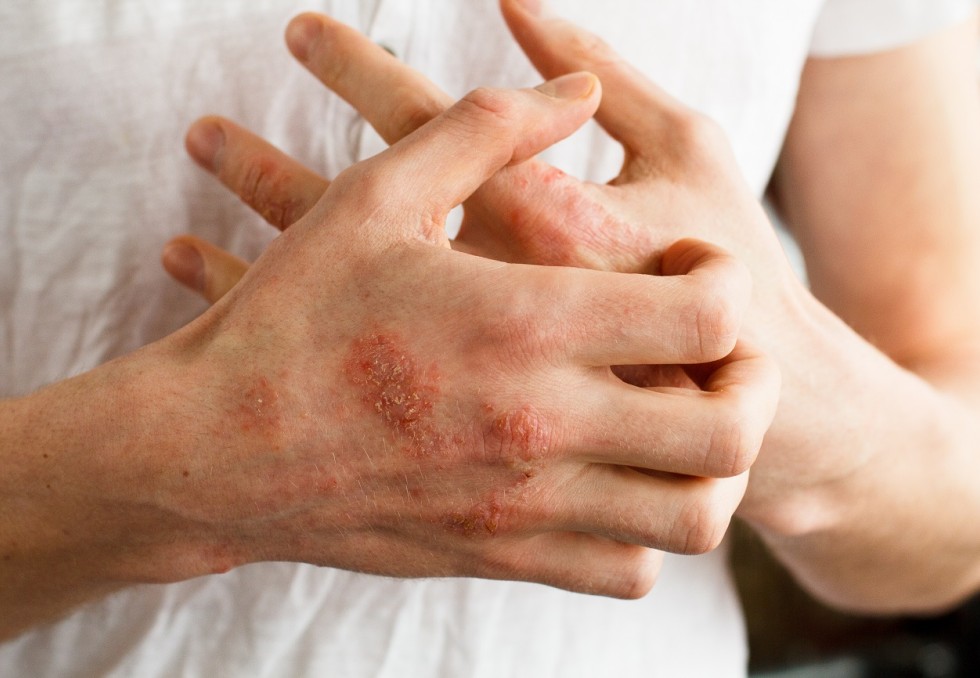
Dermatite atopique : résultats positifs avec un traitement administré 4 fois par an
La dermatite atopique (DA) pourrait bien connaitre une nouvelle évolution thérapeutique avec un nouveau traitement, développé par Sanofi, dont les derniers résultats apparaissent encourageants. Ces derniers ne semblent cependant pas à la hauteur de ce qui était attendu, entrainant une chute en bourse du laboratoire.

Ce nouveau traitement est l’amlitelimab, un anticorps monoclonal entièrement humain non déplétif des cellules T qui cible le ligand OX40 (OX40L). Développé par Sanofi, il a la particularité d’être administré toutes les quatre semaines, voire toutes les 12 semaines.
Une étude internationale de phase 3 montre, en effet, des résultats positifs, avec une amélioration de la clairance cutanée statistiquement et cliniquement significative de la clairance cutanée et de la sévérité de la maladie par rapport au placebo à la semaine 24, et une efficacité qui augmente progressivement tout au long de la période de traitement.
PLFSS 2026, MSO obligatoire... La profession médicale doit-elle se mettre en grève?

Anne SAINT-MARC FUHRER
Oui
C’est évident une grève totale historique ville hôpital MG et spé pour les hésitants c'est maintenant ou jamais et pas un seul jou... Lire plus
L’étude, nommée Coast 1, a été menées chez 601 sujets de 12 ans et plus atteints de dermatite atopique (DA) modérée à sévère. Les patients ont été randomisés ; et l’amlitelimab a été administré soit toutes les 4 semaines, soit toutes les 12 semaines.
Après 24 semaines de traitement, tous les critères d’évaluation principaux (proportion de sujets ayant clairance de la peau complète ou presque complète, réduction par rapport à l’inclusion, amélioration de 75 % ou plus du score total de l’indice de gravité et de la zone d’eczéma [EASI-75]) et secondaires clés ont été atteints ; et ce, dans les 2 groupes de traitement.
Ainsi, la proportion de patients ayant une clairance de la peau totale ou presque était de 26,5 et 29,1% (respectivement pour les groupes amlitelimab toutes les 4 et toutes les 12 semaines) contre 10,5% sous placebo. Et les score EASI- 75 était obtenu chez 46 et 50,3 % de patients traités par les 2 groupes amlitelimab, contre 27,6 % sous placebo.
En outre, L’amlitelimab a montré une bonne tolérance avec aucun nouveau problème de sécurité d’emploi identifié. Les réactions liées à l’injection du produit étaient légères. Et selon le laboratoire, les taux d’événements indésirables étaient similaires dans tous les groupes de l’étude.
Malgré ces données globalement positives, elles sont apparues plus fiables qu’attendues et ont déçu les investisseurs. En conséquence, le laboratoire Sanofi a chuté lourdement à la Bourse de Paris jeudi 4 septembre, date de publication des résultats. Pour les analystes de Jefferies, « la phase 3 de l'essai de l'amlitelimab n'a pas reproduit l'efficacité constatée lors de la phase 2 et semble moindre par rapport à d'autres médicaments », ont-ils écrit dans une note.
Cette étude Coast 1 fait partie du programme de développement clinique Oceana de l’amlitelimab. Quatre autres études de phase 3 sont en cours. Leurs résultats sont attendus d’ici 2026.
Références :
D’après un communiqué de Sanofi (4 septembre). Avec AFP
La sélection de la rédaction



